口服给药是最方便和广泛使用的药物给药方法之一。然而由于胃肠道环境恶劣,药物很难通过胃肠壁被人体吸收。口服给药面临副作用和生物利用度低的问题。多年来,人们一直在探索新的口服给药策略,以减少药物副作用并提高药物的可用性。

(图片来源于网络)
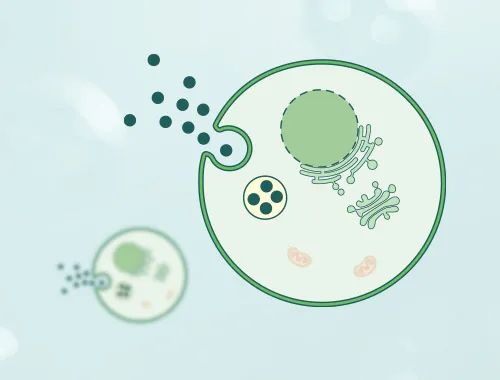
植物源性细胞外囊泡(PDEVs,Plant-derived extracellular vesicles)存在于多种植物中,具有与哺乳动物 EVs 相似的物理和化学性质。相关研究已经证明,PDEVs 可以有效地封装亲水性和疏水性药物,在恶劣的胃肠环境中保持稳定,并跨越生物屏障到达目标组织。此外,PDEVs 的生物活性使其能够与药物发挥协同治疗作用。PDEVs 的安全性和高产率表明其作为口服药物载体的潜力。
(图片来源于网络)
上海海洋大学生物制药科学系周芳教授团队在《Journal of Controlled Release》上发表题为“Plant-derived extracellular vesicles as oral drug delivery carriers“的综述文章系统的介绍了植物源性细胞外囊泡(PDEVs)的性质、制备与表征,总结论述了 PDEVs 在动物体内的靶向性、自身治疗效果以及药物运载效果,探讨了 PDEVs 作为新型药物运载体的潜力,并分析了 PDEVs 在进一步应用中面对的挑战。

(图片来源于网络)
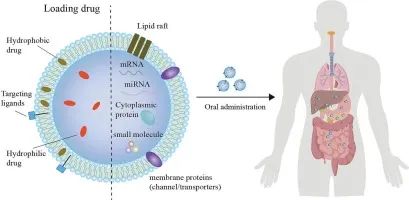
PDEVs 携带治疗剂的能力对于确定其作为药物递送载体的适用性非常重要。PDEVs 的脂质双层结构允许其将亲水药物封装在空腔中,并将疏水药物加载到脂质双层中。PDEVs 的载药方法与哺乳动物 EVs 类似,如共孵育、超声、电穿孔、冻融循环和挤压。
(图片来源于网络)
PDEVs 作为口服药物载体的优势
01安全
PDEVs 可安全用于口服给药,因为它们主要来源于长期食用或使用的植物。PDEVs 具有很高的生物相容性,口服给药后对实验动物的生理和生化参数没有显著影响。
有研究证实:生姜衍生 EVs(GDNPs)共孵育24h不影响 colon-26 和RAW 264.7 细胞的细胞活力,也不影响 Caco2-BBE 单层屏障功能的完整性。通过管饲给予 GDNPs2 (0.3 mg/小鼠)7天,促炎细胞因子水平基本稳定,未发现形态学或病理变化。
02耐受
胃肠道环境口服药物如何通过恶劣的胃肠道环境到达目标部位是限制口服药物开发的主要问题。PDEVs 在胃肠道环境中可以耐受并保持稳定。部分研究显示,GDNVs 包裹可以增强 MTX 的靶向性、抗炎效果并降低副作用;GDNVs 包裹的 siRNA-CD98 在消化道得到有效保护,并进入结肠抑制 CD98 的表达。这意味着基于 PDEVs 的口服药物递送系统有助于提高口服药物的生物利用度。在另一项研究中,槭树衍生 EVs(AELN)的封装提高了核酸的稳定性,使核酸免受酸、碱、核酸酶的降解。
03协同治疗
作为天然载体,PDEVs 比合成载体和哺乳动物 EVs 具有更大的优势,具有更低的毒性和免疫原性、更高的胃肠道稳定性和更高的产量,且继承了源植物的生物功能,如抗炎、抗癌。一项研究表明,包囊甘蓝和红甘蓝的PDEVs 都增强了 DOX 对 SW480 细胞的抑制作用,而两者单独不会抑制SW480 细胞活性。因此,PDEVs 作为口服药物载体具有协同治疗的潜力,以提高治疗效果。
有研究显示:口服给药后,大多数 PDEVs 分布在肠组织中,并被肠巨噬细胞和肠干细胞吸收,而一些 PDEVs 能够进入血流。PDEVs 的不同分布行为可能与 PDEVs 中所含的脂质有关。PA 脂质通常被鼠李糖乳杆菌(LGG)吸收,其促进 PDEVs 在肠道中的保留,而 PC 脂质主要被反刍动物球虫科吸收。此外,PDEVs 在体内的分布可能受到 PDEVs 结构的影响。
总的来说,基于 PDEVs 的口服给药系统在生物相容性、稳定性、生物分布和细胞摄取方面显示出显著的优势。此外,使用 PDEVs 递送药物可以改善药物的副作用,并发挥 PDEVs 自身的功能。这些特性使 PDEVs 能够为口服药物递送策略提供新的解决方案。目前,PDEVs 的生物医学研究仍处于起步阶段,应用于口服药物载体也将面临许多挑战。但相信随着对 PDEVs 的进一步研究,这些障碍终将在未来被克服,助力 PDEVs 在口服给药中的应用。
如需了解更多关于“肿瘤”信息
请与我们进一步联系







