前列腺癌(prostate cancer, PCa)是一种发生在男性生殖系统中的恶性肿瘤,它主要影响中老年男性的健康。据统计,前列腺癌是中国男性恶性肿瘤的第六大杀手,每年有超过11万人被诊断出患有前列腺癌,其中超过5万人因此丧命。
数据表明,几乎所有患者在接受内分泌治疗的18-36个月后,都会出现去势抵抗现象,进而发展为去势抵抗性前列腺癌 (Castration- Resistant Prostate Cancer, CRPC) 。令人遗憾的是,这类患者的中位生存期仅约14个月。
尽管目前的化疗,包括使用新型雄激素信号传导抑制剂和免疫疗法,但其死亡率仍居高不下。
近日,陆军军医大学第二附属医院泌尿外科郑霁教授/孙碧韶主治医师全面介绍了不同细胞来源的 EVs 在 CPRC 进展过程中的作用机制,总结归纳了 EVs 作为 CPRC 诊断、预后、治疗响应的生物标志物的研究进展,讨论了 EVs 作为潜在的 CPRC 治疗靶点以及药物递送系统的可能性,展望了未来 EVs 在 CPRC 治疗方面可能的应用;相关研究内容以”Role of Extracellular Vesicles in Castration-Resistant Prostate Cancer”为题在线发表在最新一期的国际肿瘤学权威期刊 Critical Reviews in Oncology/Hematology 杂志上。

(图片来源于网络)
细胞外囊泡(EVs)是由脂质层包裹的纳米级囊泡,携带大量生物大分子(如核酸、蛋白质和脂质),介导信息传递。在过去的十年中,EVs 在诊断和治疗方面都得到了广泛的应用。EVs 通过细胞间通信在病理生理过程中发挥着关键作用。靶向参与 EVs 介导的肿瘤进展(如增殖、血管生成、转移、免疫逃逸和耐药性)的关键分子是遏制 PCa 的一种潜在方法。此外 EVs 广泛分布于各种生物体液中,是无创性液体活检技术领域极具潜力的生物标志物。
EVs 在激素敏感型 PCa 向 CRPC 的转变过程中发挥重要作用,这主要归因于其复杂的分子调控。CPRC 的核心机制是重新激活雄激素受体(Androgen receptor, AR)通路及其下游通路,除了 AR 通路的再激活外,EVs 还诱导受体细胞的表型改变,导致 PCa 细胞增殖、侵袭、免疫逃逸、药物外排增加,以及 TME 对应的细胞重塑。这些改变共同促进了向去势抵抗状态的转化。
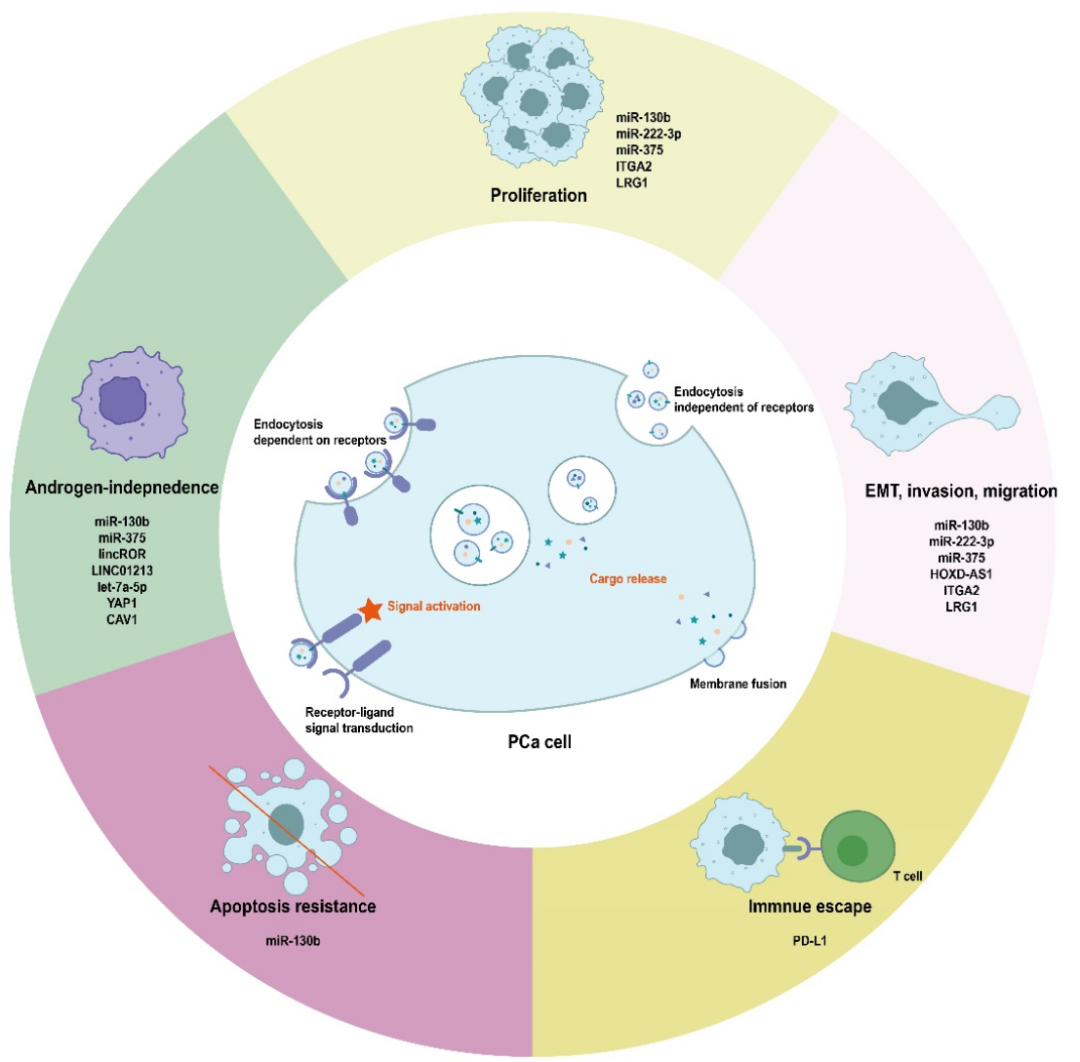
(图片来源于网络)
相较于循环肿瘤细胞与游离肿瘤 DNA,EVs 以其高丰度、长半衰期,成为一种更具潜力的生物标志物。目前已有许多研究纳入临床大样本 CRPC 队列,利用 EVs 探究新型 CPRC 诊断、进展、预后及治疗响应的标志物。本文详细介绍了不同分离方法获得的 EVs 包裹的生物标志物分子以及他们的预测效能。除了免疫捕获以外,目前 CRPC 相关研究中缺乏富集肿瘤特异性来源的 EVs 的方法,分析体液中的总 EVs 会对结果造成不同程度的偏倚。
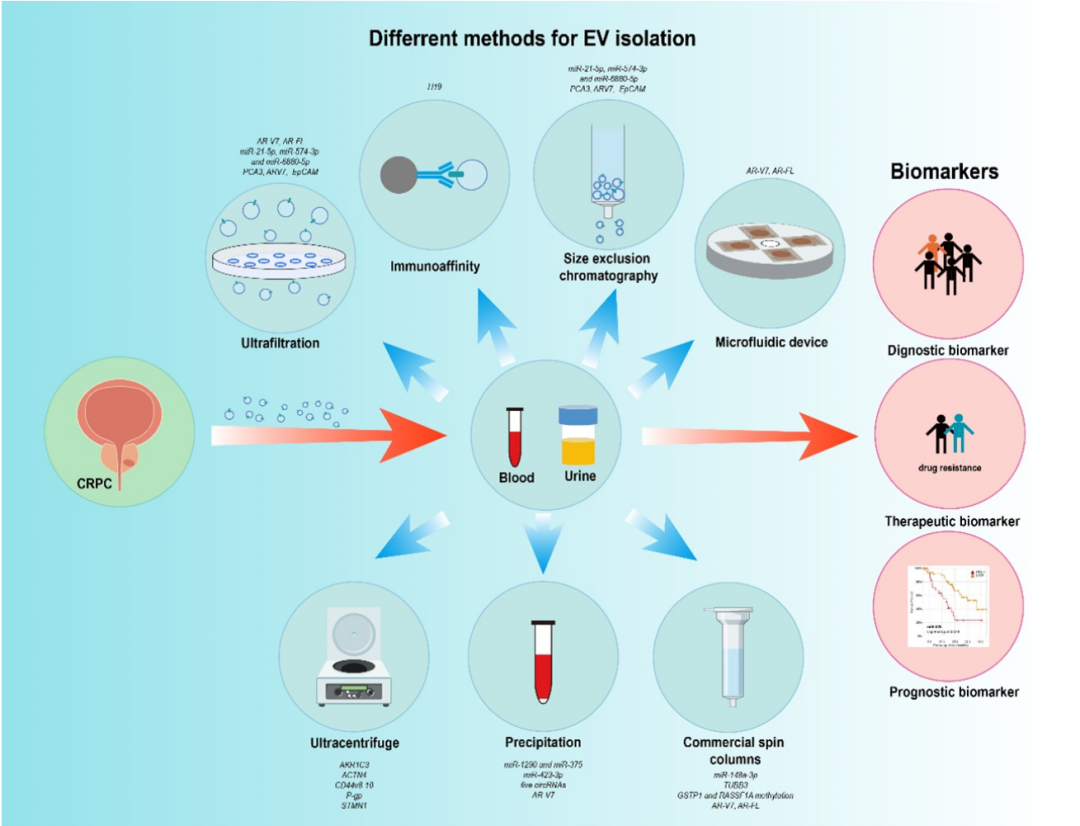
(图片来源于网络)
EVs 层面的组学分析为阐释 CPRC 的发生发展提供了新的维度,EVs 研究中鉴定出了许多新的致病分子,它们都有可能成为 CRPC 治疗的新型靶点。除此之外,EVs 具有良好的生物相容性、低免疫原性、低毒性、生物可降解性、在外周血中的半衰期长以及能够跨越各种生物屏障,这些特性让 EVs 可作为良好的药物递送载体。
如需了解更多关于“肿瘤”信息
请与我们进一步联系







